GURU VOKASI - beberapa bulan lagi ujian semester akan dilaksanakan disetiap lambaga sekolah SMA sederajat. waktunya teman teman untuk belajar giat agar bisa naik kekelas selanjutnya, berikut ini guru vokasi menulis artikel tentang bank soal Struktur Atom, Sistem Periodik dan Ikatan Kimia yang sudah diberi pembahsan maupun kunci jawabannya. jika ada beberapa pertanyaan terkait soal dibawah ini bisa ditulis dalam kolom komentar yang sudah kami sediakan.
Latihan Soal Struktur Atom, Sistem Periodik dan Ikatan Kimia
- Konfigurasi elektron dari unsur yang memiliki nomor atom 24 adalah...
- Jika atom X yang nomor atomnya 19 dituliskan konfigurasi elektronnya maka atom itu memiliki ciriciri...
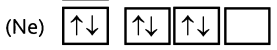
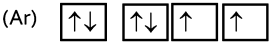
- Unsur yang mempunyai diagram elektron valensi pada keadaan dasar sebagai berikut adalah...
- Harga keempat bilangan kuantum elektron terakhir dari ₁₆S adalah....
- Dalam atom Ni dengan nomoratom 28 terdapat elektron yang tidak berpasangan sebanyak...
- Jumlah subkulit pada kulit M adalah...
- Diagram orbital yang tepat untuk elektron terakhir unsur HX adalah...
- Letak unsur X dengan nomor atom 26 dalam sistem periodik pada golongan dan periode..
- Dari beberapa unsur berikut yang mengandung:
- Terdapat empat unsur P , Q, R, S dan T yang memiliki nomor atom berturut-turut 19, 11, 13, 15 dan 17. Dari keempat unsur tersebut yang dapat membentuk ikatan ion adalah pasangan unsur atom dari ...
- Gambar rumus elektron dari amonium klorida Ikatan kovalen dan ikatan koordinasi secara berurutan adalah...
- Unsur V, W, X,Y, dan Z berturut-turut mempunyai nomor atom 2, 3, 8, 13, dan 16. Identifikasilah dari beberapa unsur tersebut yang berada dalam satu golongan adalah unsur ...
- Terdapar dua buah unsur A dan B yang memiliki nomor atom 15 dan 20, jika kedua unsur tersebut berikatan akan membntuk senyawa dengan rumus?
- Diantara kelompok senyawa di bawah iniyang semuanya mempunyai ikatan kovalen adalah ...
- Pada isotop unsur ⁶⁵₃₀Zn dan ²º⁹₈₃Bi, jumlah proton dan neutron kedua unsur tersebut berturut-turut adalah ...
A. [Ar] 4s² 3d⁴
B. [Ar] 3d⁴4p²
C. [Ar] 4s¹d⁵
D. [Ar] 3d⁶
E. [Ar] 4s² 4p⁴
Pembahasan
Konfigurasi elektron yang memiliki nomor atom 24 adalah: 1s², 2s², 2p⁶, 3s², 3p⁶ , 4s¹, 3d⁵ atau [Ar] 4s¹ 3d⁵
A. Elektron valensi = 9
B. Elektron valensi = 1
C. Elektron valensi = 7
D. Elektron valensi = 2
E. Elektron valensi = 7
B. Elektron valensi = 1
C. Elektron valensi = 7
D. Elektron valensi = 2
E. Elektron valensi = 7
Pembahasan
₁₉X = [Ar] 4s¹; ₁₉X = 2, 8, 8,1 Jadi, elektron valensinya adalah 1
A. ₆C
B. ₈O
C. ₁₅P
D. ₁₃Al
E. ₁₆S
Pembahasan
Pada gambar menunjukan bahwa unsur tersebut memiliki elektron valensi ns² np³.
₆C = 1s² 2s² 2p²
₈O =1s² 2s² 2p⁴
₁₅P = 1s² 2s²2p⁶ 3S² 3p³
₁₃AI = 1s² 2s² 2p⁶ 3S² 3p³
₁₆S=1S² 2S² 2P⁶ 3S² 3P⁴
Jadi, konfigurasi yang sesuai adalah ₁₅P.
A. n = 2, ℓ = 0, m = 0, s = −½
B. n = 3, ℓ =1, m = −1, s = −½
C. n = 3, ℓ =1, m = 0, s = −½
D. n = 3, ℓ =i, m = 0, s = +½
E. n = 3, ℓ =i, m = +1, s = +½
B. n = 3, ℓ =1, m = −1, s = −½
C. n = 3, ℓ =1, m = 0, s = −½
D. n = 3, ℓ =i, m = 0, s = +½
E. n = 3, ℓ =i, m = +1, s = +½
Pembahasan
Konfigurasi elektroni6S = 1s² 2s² 2p⁶ 3s² 3p⁴
n = 3 → terletak pada kulit M
ℓ = 1 → terletak pada subkulit p
s = → Arah panah ke bawah
A. 1
B. 2
C. 3
D. 4
E. 5
Pembahasan
Konfigurasi elektron ₂₈Ni = 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁸ Jumlah elektron yang tidak berpasangan pada orbital 3d yaitu sebanyak dua elektron.
A. 1
B. 2
C. 3
D. 4
E. 5
Pembahasan
Pada kulit M (kulit ke-3) mengandung 3 subkulit, yaitu: subkulit s mempunyai1orbital, subkulit p mempunyai 3 orbital, dan subkulit d mempunyai 5 orbital.
Pembahasan
Konfigurasi elektron dari X adalah 1s² 2s² 2p⁶ 3s² 3p⁴ atau [Ne] 3S² 3p⁴. Sesuai dengan aturan Hund, orbital dengan energi yang sama akan diisi dengan arah yang sama dahulu, kemudian elektron akan memasuki orbital secara urut dengan arah berlawanan. Jadi , diagram orbital yang tepat adalah:
A. IIA dan 6
B. VIB dan 4
C. VIB dan 4
B. VIB dan 4
C. VIB dan 4
D. VIIIB dan 3
E. VIIIB dan 4
Pembahasan
Konfigurasi elektron ₂₆X = 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁶. Jumlah elektron valensi unsurtersebut adalah 4s² 3d⁶. Jadi ,Xn terletak pada golongan VIIIB dan periode 4.
1. 20 elektron dan 20 neutron,
2. 10 elektron dan 12 neutron,
3. 15 proton dan 16 neutron,
4. 20 neutron dan 19 proton,
5. 12 proton dan 12 neutron.
Yang memiliki sifat mirip dalam sistem periodik adalah
A. 1dan 2
B. 2 dan 3
C. 2 dan 4
B. 2 dan 3
C. 2 dan 4
D. 3 dan 4
E. 1dan 5
E. 1dan 5
Pembahasan
1. 20 elektron dan 20 neutron ₂₀X = 2, 8, 8, 2 → golongan IIA, periode 4
2. 10 elektron dan 12 neutron ₁₀X = 2, 8 → golongan VIIIA, periode 2
3. 15 proton dan 16 neutron ₁₅X = 2, 8, 5 → golongan VA, periode 3
4. 20 neutron dan 19 proton ₁₉X = 2, 8, 8, 1 → golongan IA, periode 4
5. 12 proton dan 12 neutron ₁₂X = 2, 8, 2 → golongan IIA, periode 3
Dalam sistem periodik, unsur-unsur yang terdapat dalam satu golongan memiliki sifat yang sama. Jadi, unsur yang memiliki sifat yang sama adalah unsur1dan 5
A. P dan Q
B. R dan P
C. Q dan R
B. R dan P
C. Q dan R
D. Q dan T
E. T dan S
Pembahasan
Susunan konfigurasi elektron masing-masing unsur:
₁₉P = 2, 8, 8,1→ golongan IA (logam)
₁₁Q = 2, 8,1→ golongan IA (logam)
₁₃R = 2, 8, 3 → golongan IIIA (logam)
₁₅S = 2 , 8, 5 → golongan VA (nonlogam)
₁₇T = 2, 8,7 → golongan VIIA (nonlogam)
Ikatan ion dapat terbentuk dari:
- Unsur logam dengan unsur nonlogam
- Unsuryang mudah melepaskan dan menarik elektron
Jadi, ikatan ion dapat terjadi antara Q dan T.
A. 1 dan 2
B. 1 dan 3
C. 2 dan 5
B. 1 dan 3
C. 2 dan 5
D. 3 dan 5
E. 1 dan 4
Pembahasan
Nomor 1= Ikatan kovalen
Nomor 2 = ikatan kovalen koordinasi
Nomor 3 = ikatan kovalen
Nomor 4 = ikatan kovalen
Nomor 5 = ikatan kovalen
Jadi , ikatan kovalen dan kovalen koordinasi secara berurutan adalah1dan 2.
A. Wdan Z
B. X dan Y
C. U dan X
B. X dan Y
C. U dan X
D. Xdan Z
E. Vdan Y
Pembahasan
Susunan konfigurasi elektron masing-masing unsur:
₂V = 2 → golongan VIIIA
₃W = 2, 1 → golongan IA
₈X = 2, 6 → golongan VIA
₁₃Y = 2, 8, 3 → golongan IIIA
₁₆Z= 2,8,6 → golongan VIA
Jadi, yang berada dalam satu golongan adalah X dan Z.
A. XY
B. XY₂
C. X₃Y₂
B. XY₂
C. X₃Y₂
D. X₂Y₃
E. XY₃
Pembahasan
Unsur ₁₅X memilikl konfigurasi elektron 1, 8, 5 (golongan VA kecenderungan mengambil 3 elektron)
Unsur ₂₀Y memiliki konfigurasi elektron 2, 8, 8, 2 (golongan IIA kecenderungan mlepaskan 2 elektron)
Sehingga:
X + 3e⁻ →X ³⁻
Y → Y²⁺ + 2e⁻
2X³⁻ + 3Y²⁺ → X₂Y₃
Jadi, jawaban yang tepat adalah X₂Y₃
A. KCI, NaCI, dan HCI
B. NH₃, CaO, dan K₂O
B. NH₃, CaO, dan K₂O
C. HCI, SO₂, dan NH₃
D. KBr, NaCI, danCaBr₂
E. H₂O, Na₂O, dan N₂O₅
D. KBr, NaCI, danCaBr₂
E. H₂O, Na₂O, dan N₂O₅
Pembahasan
Ikatan kovalen adalah ikatan yang terbentuk antara unsur nonlogam dan unsur nonlogam. Sedangkan ikatan ion terbentuk antara unsur logam dan unsur nonlogam. Unsur-unsur yang terbentuk dari nonlogam dan nonlogam antara lain HCI, NH₃, SO₂, H₂, dan N₂O₅. Sedangkan, KCI, NaCI, CaO, K20, KBr, dan CaBr₂ merupakan unsur-unsur yang terbentuk dari logam dan nonlogam.
Jadi,jawaban yang tepat adalah HCI, SO₂, dan NH₃
A. 30 dan 30; 83 dan 126
B. 35 dan 30; 83 dan 209
C. 30 dan 35; 83 dan 126
D. 30 dan 35; 83 dan 129
E. 30 dan 35; 83 dan 209
B. 35 dan 30; 83 dan 209
C. 30 dan 35; 83 dan 126
D. 30 dan 35; 83 dan 129
E. 30 dan 35; 83 dan 209
Pembahasan
Unsur ⁶⁵₃₀Zn → Proton = 30, Neutron = 65- 30 = 35
Unsur ²º⁹₈₃Bi → Proton = 83, Neutron = 209 - 83 =126
Jadi, Jawaban yang tepat adalah 30 dan 35; 83 dan 126
TERIMAKASIH TELAHN BERKUNJUNG DI WEBSITE KAMI, SELALU KUNJUNGI WEBSITE guruvokasi.com UNTUK MENDAPATKAN ARTIKEL TENTANG MATA PELAJARAN KIMIA. BAIK TENTANG MATERI MAUPUN TENTANG BANK SOAL KIMIA
MATERI DAN CONTOH SOAL LAINNYA
Rangkuman Materi dan Perubahan Unsur Kimia
Ringkasan Materi Kimia Sistem Periodik Unsur
Ringkasan Materi Perkembangan Teori Model Atom
Rangkuman Materi Bilangan Kuantum
Rangkuman Materi Konfigurasi Elektron
20 Soal dan Kunci Jawaban Struktur Atom
30 Latihan dan Kunci Jawaban Soal Struktur Atom
Latihan Soal Struktur Atom, Sistem Periodik dan Ikatan Kimia |
Ringkasan Materi Kimia Sistem Periodik Unsur
Ringkasan Materi Perkembangan Teori Model Atom
Rangkuman Materi Bilangan Kuantum
Rangkuman Materi Konfigurasi Elektron
20 Soal dan Kunci Jawaban Struktur Atom
30 Latihan dan Kunci Jawaban Soal Struktur Atom
Latihan Soal Struktur Atom, Sistem Periodik dan Ikatan Kimia |














Tidak ada komentar:
Posting Komentar